康晓征医生的科普号
- 精选 食管癌术后吻合口瘘诊疗现状调查及常用处理方法
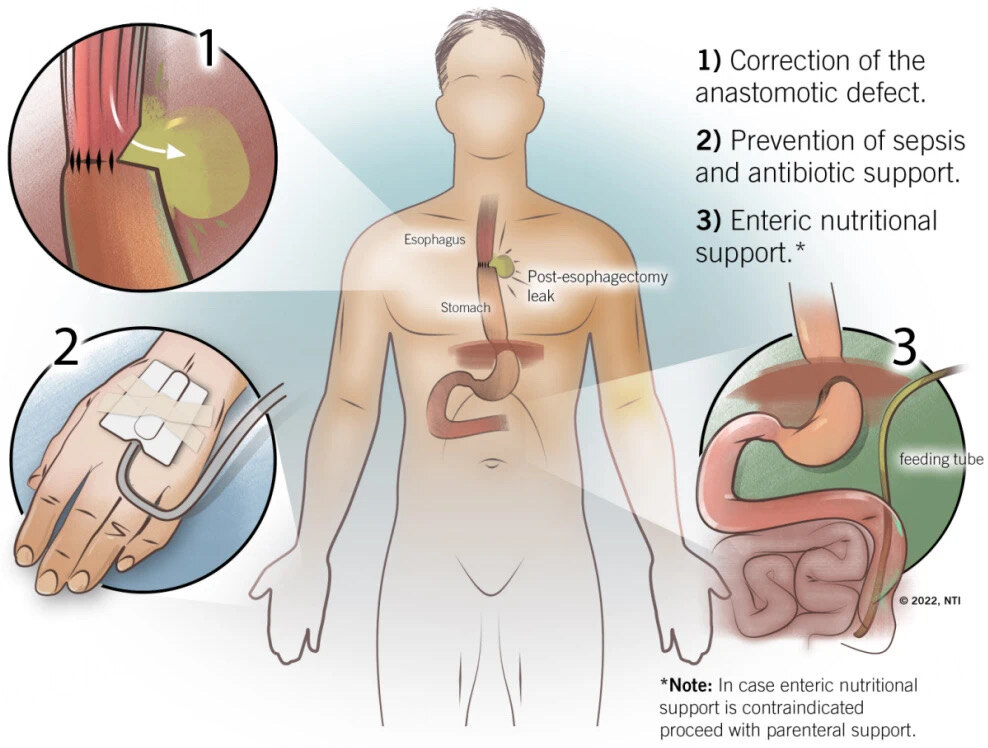
调查研究,是我们党的传家宝,是一代代中国共产党人从胜利走向胜利的谋事之基、成事之道。为了回答本文问题,是必须要进行广泛调查的。没有调查,就没有发言权,更没有决策权。吻合口瘘是食管癌术后主要外科并发症之一,涉及临床表现繁多,处置方法也因人而异,尚无公认规范化标准。因此,有必要进行全行业范围内的调查研究,归纳梳理吻合口瘘不同症状的临床意义,比较不同处理干预方法的有效性差异。近期,国外学者开展了一项全球范围的横断面调查,共计71家食管外科中心参与,回顾了2011年至2019年期间食管外科术后吻合口瘘病例的治疗资料。比较了三种不同吻合口瘘临床表现及治疗策略的利弊:(1)管状胃血供良好,无胸内引流前提下,仅行介入治疗对比对症支持治疗;(2)直接针对瘘口闭合对比胸内引流的各种处置方法;(3)管状胃已发生缺血坏死的前提下,瘘口旷置,代食管旁路重建术对比胸内引流处理。主要研究终点为术后90日内死亡率。该调查结果显示,共计1508例食管术后吻合口瘘患者纳入分析,425例(28.2%)仅有局部症状,548例(36.3%)具有胸腔内症状,145例(9.6%)出现管状胃缺血坏死征象,264例(17.5%)由于病历记录信息缺失进行了多重补填处理,126例(8.4%)被排除。经过倾向匹配评分法剔除混杂因素分析后,针对(1)型吻合口瘘的两种处置方法的90日内死亡率无统计学差异(风险差3.2%,95%CI-1.8%~8.2%);针对(2)型吻合口瘘,瘘口闭合对比胸内引流的围术期死亡率也无显著差异(风险差5.8%,95%CI-1.2%~12.8%);针对(3)型吻合口瘘,旷置术与引流术的围术期死亡率差异同样无显著差异(风险差0.1%,95%CI-21.4%~1.6%)。总之,采用创伤性越小的处置方式,相关并发症风险越低。参考文献:UbelsS,VerstegenMHP,KlarenbeekBR,etal.Treatmentofanastomoticleakafteroesophagectomyforoesophagealcancer:large,collaborative,observationalTENTACLEcohortstudy.BrJSurg.2023;110(7):852-863.谈及食管癌切除重建的不同吻合技术,尽管回顾性多中心队列研究常提供不同技术之间的吻合口狭窄或吻合口瘘发生率差异,然而笔者认为同主刀医师擅长方式及熟练程度密切相关,孰优孰劣难以简单地下定论。线上咨询常问到了的食管癌术后吻合口处理原则包括:(1)尽量修补瘘口缺损;(2)充分地外科引流,预防性或治疗性抗生素药物治疗;(3)充足的肠内营养支持治疗。参考文献:JärvinenT,Cools-LartigueJ,RobinsonE,etal.Hand-sewnversusstapledanastomosesforesophagectomy:Wewillprobablyneverknowwhichisbetter.JTCVSOpen.2021;7:338-352.
 康晓征 副主任医师 医科院肿瘤医院 胸外科544人已读
康晓征 副主任医师 医科院肿瘤医院 胸外科544人已读 - 精选 【经典问答】纵隔肿瘤需要手术吗?哪种适合微创手术?
蜂蝶纷纷过墙去,却疑春色在邻家。医疗服务评价离不开患者满意,这是近日门诊几个病人咨询后一点感悟。言归正传谈纵隔肿瘤,首先追本溯源纵隔并非器官,却是胸腔内诸多重要脏器之间隙。医学上将纵隔进行分区,分为上、中、下、前、后区(图1)。图1. 纵隔分期示意图 纵隔肿瘤来源繁多,既有原发性也有转移性疾病。常见原发性纵隔肿瘤包括胸腺瘤、畸胎瘤、神经鞘瘤等,转移性肿瘤则根据原发灶不同表现更加变化莫测,例如结肠癌纵隔淋巴结转移(图2)。早期纵隔肿瘤常无明显临床症状,仅仅体检偶然发现。直到肿瘤增大压迫周围脏器,可能导致疼痛、胸闷、心悸、声音嘶哑、进食困难、头面肿胀等症状或体征。目前临床评估纵隔肿瘤的常用方法为增强CT扫描(图3)。一旦发现纵隔肿物,需要进一步排查是否存在胸外病灶(以淋巴瘤等血液系统肿瘤多见),推荐全身PET-CT(图4)。为了评估手术指征,尤其术前估计外科切缘是否安全,还需要依靠MRI技术分辨肿瘤边界的软组织层次。术前确诊需要组织病理学评估,对于巨大、多灶、边界不规则的纵隔肿瘤,穿刺活检有创操作是必需的。图2. 纵隔转移性结肠癌参考文献:Yamamoto Y, Kodama K, Ide Y, Takeda M. Thymic and Mediastinal Lymph Node Metastasis of Colon Cancer. Ann Thorac Surg. 2017;103(1):e13-e15.图3. 巨大纵隔肿瘤增强CT影像图4. 纵隔肿瘤CT与PET-CT影像 从传统外科角度讲,完全显露纵隔术野对于患者术中安全操作是重要保障,也使得术者能够更加有信心完成复杂高风险操作(图5)。然而,充分显露术野势必要“开大刀"——纵劈胸骨入路(图6),适合巨大瘤体外侵明显(侵犯周围动静脉主干),术后需要行胸骨内固定术(图7)。为了缓解术后疼痛,加速术后康复,近年来胸外科改良了手术入路,例如经腋下、剑突下微创切口(图8、9)。图5. 纵隔外科完全显露术野示意图图6. 纵劈胸骨正中开胸示意图图7. 胸骨内固定术示意图图8. 保留肌肉腋下微创切口示意图图9. 经剑突下单孔操作示意图 上纵隔肿物毗邻重要血管、神经、器官最多(图10),若肿瘤外侵则需要做血管成形术,甚至人工血管置换术,因此目前仍无法实施微创手术方式。术前明确病理诊断后,通过新辅助放化疗、介入栓塞等方法缩小病灶,再行手术切除则可以降低出血损伤风险,同时也提高根治性切除机会,避免术后复发转移。总之,纵隔手术应首先顾全肿瘤学无瘤原则与外科学安全原则,其次再追求减少创伤,提升术后生活质量,切不可舍本逐末。上述先决条件下,剩下考验外科医师的就是耐心与毅力了,逢山开道,遇水架桥。图10. 上纵隔胸廓入口解剖示意图
康晓征 副主任医师 医科院肿瘤医院 胸外科3671人已读 - 精选 【经典问答】烧心与食管癌
现代社会成年人的世界里,压力无孔不入,终日辛劳奔波。孟子云:劳心者治人,劳力者治于人。人生不满百,常抱千岁忧。然而,许多劳心者们终日受到“烧心”困扰。所谓烧心,是西方医学症状名词“heartburn”舶来品,指出现于胸骨后的“烧灼感”不适,通常令医生首先联想到上消化道反流性疾病(简称GERD)。然而,并非所有烧心症状均系GERD,就诊时医生还需要鉴别心肌缺血导致的不稳定心绞痛,膈肌裂孔疝,下纵隔肿瘤等疾病,本文仅阐述最常见的GERD。图1. GERD发病机制及处理示意图(参考文献:Maret-Ouda J, Markar SR, Lagergren J. Gastroesophageal Reflux Disease. JAMA. 2020;324(24):2565.) 如图1所示,GERD发病原因多与食管下括约肌(简称LES)张力减弱有关,后者类似于“瓶塞”或“开关”,司职进食后防止胃内容物反流入下段食管,这其中就包括参与食物消化的胃酸。导致LES张力减弱的危险因素包括肥胖,吸烟,家族遗传等。强酸性胃液常反流至咽喉产生瞬间呛咳,长期反流则导致出现夜间呼吸困难、喘憋、气促、失眠等症状。此外,高频次强酸反流会反复损伤食管黏膜,在不断损伤修复过程中发展为Barrett食管,即食管下段黏膜正常鳞状上皮细胞被柱状上皮细胞替代。虽为人体自我保护机制,但却可能演变为癌症,发展为食管胸下段癌或者食管胃交接癌,或者俗称“贲门癌”。 通常治疗GERD分为三个阶梯:1. 生活方式改变,包括减重、戒烟、安眠等,其中如何消除焦虑情绪,避免纵欲,还需要患者个人修炼“养心”;2. 消化内科抑酸药物——质子泵抑制剂(简称PPI),包括奥美拉唑、兰索拉唑等,PPI抑制胃内泌酸细胞产生胃酸,从而减少强酸性胃液反流,数周试验性PPI治疗后若烧心症状缓解,则可确诊GERD;3. 对于顽固性GERD,选择性实施外科治疗,即通过胃底折叠术,将近端胃成型包绕下段食管,人工制造机械性“开关”防止胃酸反流。近期一项GERD治疗的随机对照研究结果公布,共计366例GERD患者参与筛选,经常规PPI治疗无效的78例患者按照1:1:1比例被随机分为两组:A:胃底折叠术;B:奥美拉唑+巴氯芬组;C:奥美拉唑+安慰剂组,最终结果表明联合外科治疗成功率显著优于联合PPI药物治疗(67% vs 28%, P = 0.007)以及单纯PPI药物治疗(67% vs 12%, P < 0.001)(图2)。图2. GERD治疗随机对照研究方案及结果示意图(参考文献:Spechler SJ, Hunter JG, Jones KM, et al. Randomized Trial of Medical versus Surgical Treatment for Refractory Heartburn. N Engl J Med. 2019;381(16):1513-1523. ) 孟子曰:“养心莫善于寡欲。其为人也寡欲,虽有不存焉者,寡矣;其为人也多欲,虽有存焉者,寡矣。” 为了避免长期烧心导致食管癌或食管胃交界癌发生,患者自身需要修炼“养心”。
康晓征 副主任医师 医科院肿瘤医院 胸外科1303人已读 - 精选 【经典问答】食管癌前病变何时恶变?食管癌治疗后能够多久?
一片芳心千万绪,人间没个安排处。当终于鼓起勇气做了胃镜检查提示Barrett食管时,是不是食管癌?胃癌?会不会恶化?闻“癌”色变,日夜困扰着众多上消化道疾病患者。随着当前我国生活水平不断改善,营养过剩、肥胖问题带来的副产品——食管胃反流性疾病(简称GERD)近年来呈现逐渐抬头趋势。Barrett食管即是GERD导致食管正常黏膜发生的病理改变,诊断需要经过内镜检查明确。内镜下可见原有食管下段粘膜的鳞状上皮被柱状上皮替代(图1、2)。导致Barrett食管的危险因素包括:高龄、肥胖、男性、吸烟、红肉类为主饮食习惯、长期烧心症状、30岁以前即确诊GERD、食管裂孔疝、糜烂性食管炎、代谢异常综合征、家族性Barrett食管疾病史等,上述因素也多为食管胸下段腺癌或食管胃交界癌的危险因素(图3)。图1. 上消化道内镜检查示意图图2. Barrett食管病理改变示意图图3. Barrett食管及食管腺癌的危险与保护因素列表参考文献:Spechler SJ, Souza RF. Barrett's esophagus.N Engl J Med. 2014;371(9):836-845. 患者一旦发现Barrett食管,主诊医生通常会根据内镜下活检病理结果进行分级诊疗。简而言之,根据病理活检组织病理学不典型增生的程度,分为(1)无不典型增生,(2)低级别不典型增生,(3)可疑高级别不典型增生或粘膜内癌。对于(1)则仅需要每3~5年复查胃镜随诊即可;(2)经高年资病理科医师确认后,需要在6~12个月后复查,或者内镜下黏膜切除术;(3)需要积极进行内镜下黏膜切除术。具体诊疗流程图见图4。图4. Barrett食管诊疗流程简图参考文献:Spechler SJ, Souza RF. Barrett's esophagus.N Engl J Med. 2014;371(9):836-845. 现代基因测序技术可协助医生进一步监察Barrett食管疾病进展。近期一项临床前研究结果显示,运用全基因组测序技术,可将长期内镜随访患者的连续活检组织样本进行深入分析,协助临床区分进展型(P)与非进展性(NP)患者,进而个体化随诊或治疗(图5、6)。图5. 共计88例Barrett患者完成长达15年连续内镜随诊活检图6. 根据基因预测分型开展个性化诊疗策略参考文献:Killcoyne S, Gregson E, Wedge DC, et al. Genomic copy number predicts esophageal cancer years before transformation.Nat Med. 2020;26(11):1726-1732. 确诊食管癌后如何制定下一步治疗方案,需要医生和患者/家属共同商讨,这其中就涉及对不同治疗策略损耗比(cost-effective ratio)的权衡,兼顾“算命”与“花钱”。大型食管癌诊疗中心医生经验丰富,接触多模态诊疗病例数多,会更有助于患者决策。随着我国食管癌患者逐渐向大中心集约趋势日益明显,食管癌诊疗专业团队对共同决策的影响也越发重要。西方先进国家已经通过建立国家性或区域性临床数据库,构建临床预测模型以指导医患共同决策。典型案例是荷兰多中心临床数据库SOURCE,通过收集2015年~2018年期间荷兰全国范围内确诊食管癌与胃癌病例数据,可以构建不同治疗模式下生存预测临床模型(图7)。这样则将医生个人经验进行了延展,也可为患者开放进行公共访问查询。我国食管癌病例数据收集与临床模型构建也在进行中。图7. 荷兰多中心SOURCE数据库构成及变量模型示意图参考文献:van den Boorn HG, Abu-Hanna A, Haj Mohammad N, et al. SOURCE: Prediction Models for Overall Survival in Patients With Metastatic and Potentially Curable Esophageal and Gastric Cancer.J Natl Compr Canc Netw. 2021;19(4):403-410.
康晓征 副主任医师 医科院肿瘤医院 胸外科1886人已读 - 精选 【经典问答】食管癌纵隔淋巴结转移做手术还有意义吗?
善除害者察其本,善理疾者绝其源。从解剖结构角度讲,食管位于胸腔内各器官的“C”位(图1),因其位置深在故不易于早期发现病患。若非体检意识强并且亲历体验现代胃镜早诊筛查,食管癌患者一旦确诊则多为局部晚期甚至晚期。食管癌病变可能通过食管粘膜下交织贯通的淋巴管网发生区域甚至远隔淋巴结转移(图2),临床上难以捕捉踪迹,区域淋巴结转移也是食管癌疗效提升的瓶颈之一。图1.食管及邻近器官解剖示意图图2.食管癌不同分期区域及远隔转移示意图食管切除与重建外科手术是人类历史上最早出现的食管癌根治方法,现代食管外科技术发展已逾百年(以1915年Torek报道首例同期食管切除重建治疗食管癌为里程碑)。目前已发展成为一套较成熟的体系,以“微创外科”理念引领食管外科(简称MIE)发展至今(图3、4),围术期并发症已经显著降低。然而,“替代食管”重建技术由于缺乏满意的人造材料,因此仍沿用着“自身器官代食管”理念,诸多脏器中以胃代食管应用最多(图5、6、7)。图3.微创食管外科腹部切口示意图图4.微创食管外科胸部切口示意图图5.腹腔镜下游离胃示意图图6.腹腔镜下“管状胃”制作示意图图7.“管状胃”与残食管吻合示意图本文重点提及食管癌外科治疗中转移性淋巴结的治疗问题,如图8所示,常见区域淋巴结被分站定义,用于临床病理分期、预后预测及治疗策略制定。区域淋巴结分布于患者双侧锁骨上野、胸野、腹野(简称三野),是食管外科术前系统性或选择性淋巴结清扫是重要的组成部分,也兼顾“分期”及“治疗”两个任务。食管癌术中“两野”或“三野”淋巴结清扫的数目、站数、完整性是评价食管外科质量的重要指标之一。根据我国2009年~2014年统计国内食管癌大中心8181例患者的术后生存结果,术后1年、3年、5年总生存率分别为82.6%、61.6%及52.9%。(参考文献:MaoYS,GaoSG,WangQ,etal.Analysisofaregistrydatabaseforesophagealcancerfromhigh-volumecentersinChina.DisEsophagus.2020;33(8):doz091.)可以说,外科治疗依旧是食管癌最重要的治疗方法,历久弥新,毋庸置疑。图8.国际TNM分期食管癌淋巴结分站示意图与此同时,随着肿瘤多学科综合治疗理念不断深入,食管外科也同放疗、化疗不断融合,针对区域淋巴结转移的可切除局部晚期食管癌采用了多模式综合治疗方案,即术前新辅助放化疗后再实施手术切除。最具代表性的国外多中心随机对照研究CROSS近期公布了十年随访结果,术前经过放化疗治疗后再行手术治疗组患者的十年生存率的绝对优势高达13%(38%vs25%);以手术主导的综合治疗模式可将术后死亡风险降低40%(HR,0.60;95%CI,0.46to0.80)(图9),并且不会随着时间推移而衰减。(参考文献:EyckBM,vanLanschotJJB,HulshofMCCM,etal.Ten-YearOutcomeofNeoadjuvantChemoradiotherapyPlusSurgeryforEsophagealCancer:TheRandomizedControlledCROSSTrial.JClinOncol.2021;39(18):1995-2004.)图9.多学科综合治疗模式的生存优势基于最新更新的CROSS研究结果,只要有可根治性切除的机会,即便“潜在”或者“边界”可切除疾病,均应该积极运用多学科综合治疗手段实施降期后向手术转化。君子之学必日新,日新者日进也。食管外科专业只有敞开双臂拥抱肿瘤学进展,同多学科协作共赢,才能更好地发展为患者服务。
康晓征 副主任医师 医科院肿瘤医院 胸外科5203人已读 - 精选 食管癌术前放化疗后完全缓解还需要手术吗?
目前对于局部晚期食管癌患者,术前诱导放化疗联合手术是标准的治疗模式。诱导治疗后若病理完全缓解,简单地讲就是肿瘤细胞完全被杀灭了,则预示着术后获得长期生存(包括总生存及无疾病生存)的几率大大提高。然而,大约三分之一病理完全缓解的患者中仍有复发,不仅不能省去外科手术,术后严密随访也不同忽视。诊疗关键在于如何确定复发高风险的完全病理缓解食管癌患者。近期,美国纽约纪念斯隆凯特琳癌症中心回顾了233例II~III期术前根治性放化疗获得完全病理缓解的患者资料,发现其中61例患者复发(其中腺癌43例,鳞癌18例);腺癌及鳞癌的5年累积复发风险率分别为28%(95%CI,21 - 35)及 31%(95%CI,19 - 43);低分化癌是局部复发的独立预后危险因素(HR 2.28,P = 0.009);食管鳞癌患者术后复发多见于局部范围,而食管腺癌更倾向远处转移。 近年来食管术前诱导放化疗的数据不断积累,放化疗后食管鳞癌的病理完全缓解率可达40%。上述研究也提醒我们不应盲目乐观,即便获得病理完全缓解也并不意味着治愈。对于可手术食管癌仅行诱导放化疗剂量以期避免手术是不安全的,并且放化疗后如何确认完全缓解也缺乏有效的方法,因此手术仍不能被省略掉,如何提高围术期安全性及优化术后管理依然是今后临床研究的方向。鉴于鳞癌与腺癌的复发转移模式不同,需要更加强调针对食管鳞癌更加广泛的区域淋巴结清扫;针对食管腺癌分期检查添加颅脑核磁共振可能是有必要的。参考文献:Barbetta A, Sihag S, Nobel T, et al. Patterns and risk of recurrence in patients with esophageal cancer with a pathologic complete response after chemoradiotherapy followed by surgery. J Thorac Cardiovasc Surg. 2018.
康晓征 副主任医师 医科院肿瘤医院 胸外科4853人已读 - 经典问答 【经典问答】如何判断纵隔肿瘤需要外科切除?
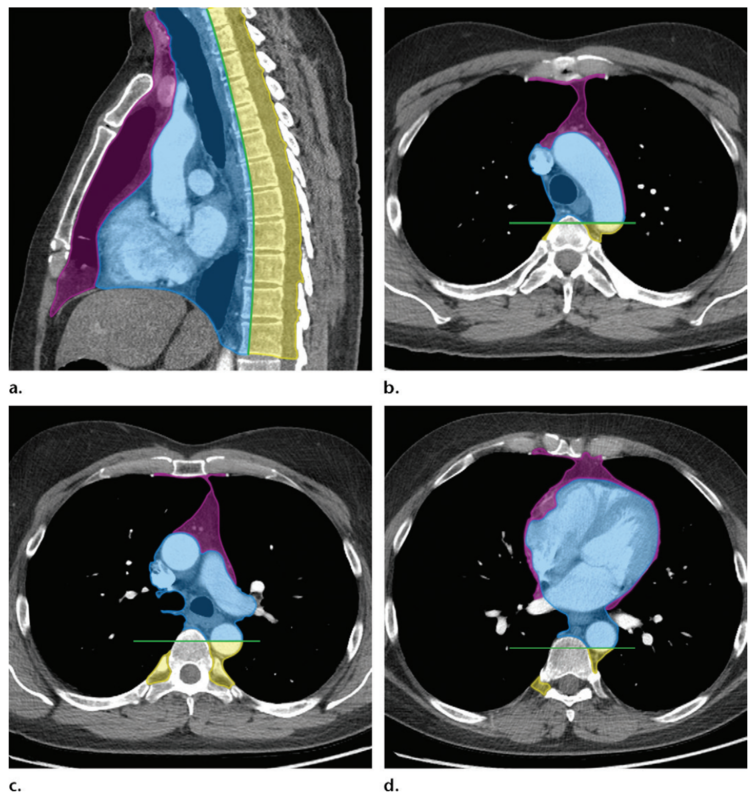
随着胸部CT被广泛应用于肺部疾病鉴别诊断及常规体检,纵隔肿瘤检出数目也逐渐随之升高。排除流行性呼吸系统病毒感染爆发影响,每年纵隔肿瘤患者常在入学、入伍、入职体检时段检出就医,故也成为“高考瘤”、“入伍瘤”或“入职瘤”。根据解剖部位分布,纵隔肿瘤分为前、中、后;上、中、下区域。鉴于纵隔肿瘤疾病种类繁多,涉及胸腺来源、胸膜来源、神经来源、胚胎来源(畸胎瘤)、甲状腺来源、骨髓来源、淋巴系统来源等多个器官或系统,故鉴别诊断较为困难,多数情况下确诊需要依靠切除活检后的病理诊断结果。如果条件允许,术前CT或者超声引导下细针穿刺活检看提供重要诊断依据。中青年人群是纵隔肿瘤好发群体,初次发现建议结合多模态影像学检查评估,主要指增强CT联合MRI。此外,全身PET-CT有助于明确胸外病灶分布,常协助临床医生寻找原发肿瘤,或者辅助诊断淋巴瘤。以胸腺上皮来源肿瘤(俗称胸腺瘤)为例,动态观察期间发生显著变化,或者初诊时影像学评估边界不清则应警惕恶性肿瘤可能。尽早外科干预以避免肿瘤恶化外侵导致无法根治性切除。通常情况下,直径<1cm的纵隔肿瘤可考虑定期随诊,动态评估肿瘤变化,推断肿瘤生物学行为特征以鉴别良恶性。少数情况下,也可以通过微创外科方式完整切除以清除疾病与精神负担,然而外科干预的利弊需要术前充分同患者及家属交流,获得知情同意。上图病例则是1例少见的青年型早期胸腺鳞癌患者,经微创外科治疗后术后病理诊断为I期胸腺鳞癌,术后定期随诊无复发转移征象。个人经验更倾向通过动态观察评估肿瘤影像学倍增时间以辅助诊断,唯有敬畏肿瘤疾病本身,在先进科技的“仙人指路”下,充分发挥各个棋子的特色优势,才能实现“帅士无损,所向无敌”。
 康晓征 副主任医师 医科院肿瘤医院 胸外科46人已读
康晓征 副主任医师 医科院肿瘤医院 胸外科46人已读 - 经典问答 【经典问答】局部晚期食管癌经过新辅助治疗后能否免于手术?
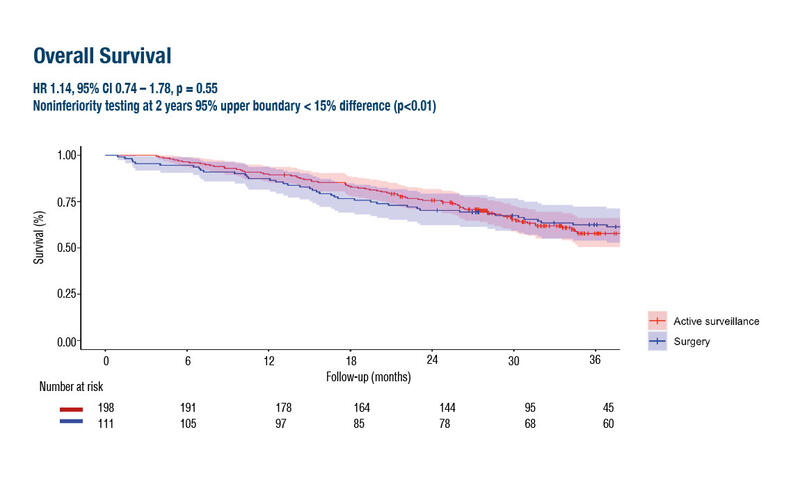
据统计约三分之一的食管癌患者在接受新辅助化放疗(nCRT)序贯根治性切除术后会获得病理完全缓解(pCR)。对于nCRT后再分期评估达到临床完全缓解(cCR)患者而言,避免食管胃切除,通过密切临床随诊以保留器官,进而保障生活质量尽可能不受影响可能是另一种选择。近期,一项非劣效性、阶梯式分组、随机试验(SANO研究)结果公布。经多模态临床评估后,获得cCR(即nCRT治疗后6周及12周后仍未发现肿瘤残留证据)食管癌患者接受密切内镜随访(仅在确诊局部复发时再实施手术)或者标准食管癌手术。SANO研究的主要终点是自诊断cCR之日起的总生存期(OS)。非劣效性的定义是两年后食管癌患者的死亡率危险比(HR)<1.77;次要终点是手术结果、无病生存期(DFS)、远处转移率和生活质量(HRQOL,经EORTCQLQ-C30量表评估)。最终共有198名患者入组密切随访,111名患者入组标准食管癌手术。密切随访组的中位随访时间为34个月,标准食管癌手术组为50个月。密切随访的术后OS不劣于标准食管癌手术(HR0.88,95%上限1.40,P=0.007)。在密切随访期间,69名患者(35%)持续保持cCR,96名患者(48%)发生了局部复发,33名患者(17%)发生了远处转移。两组患者的R1发生率均为2%,术后90天死亡率分别为4%(密切随访)和5%(标准食管癌手术)。密切随访组的中位DFS为35个月(95%CI31-41个月),而标准食管癌手术组为49个月(95%CI38-NA)(HR1.35,95%CI0.89-2.03,P=0.15)。在接受nCRT治疗30个月后,43%入组密切随访的患者出现远处转移,而34%接受标准手术的患者出现远处转移(OR1.45,95%CI0.85-2.48,P=0.18)。从统计学角度评价,密切随访组患者在nCRT结束后6个月(P=0.002)和9个月(P=0.007)时的HRQOL明显更好。尽管SANO研究结果令人兴奋,但是冷静注意到那些临床再评估未获得cCR的广大患者多数在nCRT后10周内接受了根治性手术。未来若要将SANO模式应用于临床,我们可能仍需要评估上述患者的疗效。为此,我们可能需要开展一项新的随机临床研究,对比SANO模式与nCRT后6周进行食管癌手术的标准疗法进行比较,HRQOL与OS都将是重要的临床终点。参考文献VanderWilkBJ,etal.Neoadjuvantchemoradiotherapyfollowedbysurgeryversusactivesurveillanceforoesophagealcancer(SANO-trial):aphase-IIIstepped-wedgeclusterrandomisedtrial.ESMOCongress2023,LBA75.
 康晓征 副主任医师 医科院肿瘤医院 胸外科63人已读
康晓征 副主任医师 医科院肿瘤医院 胸外科63人已读 - 经典问答 【经典问答】食管癌患者都会有梗噎感吗?
进食后梗噎感、食物停滞感、胸骨后闷胀感等主诉是食管疾病(包括恶性与良性肿瘤)常见临床症状,并且短期内(通常1-3个月)进行性加重多提示恶性肿瘤可能性大。患者常采用配合饮水、少食、跳动辅助进食。然而,并非所有食管癌患者初始症状都是吞咽困难,梗阻症状出现时间与食管肿瘤病理学大体类型有关系。食管癌指食管黏膜上皮或者间叶组织来源的恶性肿瘤,常见病理类型包括鳞状细胞癌(我国发病率最高)、腺癌、肉瘤样癌、神经内分泌癌等。内镜下评估活检获取肿瘤组织进行病理学诊断是鉴别诊断的重要依据。根据病理学大体标本分型,局部进展期食管恶性肿瘤生长方式不同,被分为髓质型、蕈伞型、溃疡型、缩窄型及腔内型。其中,缩窄型导致食管管腔狭窄,阻碍食糜通过,患者主诉梗噎感最为明显。不同大体病理类型的食管恶性肿瘤在影像学评估中的特征也迥异,临床评估需要结合内镜学与影像学多模态综合分析,并且经过抗肿瘤治疗后再分期评估同样需要多维度评估。
 康晓征 副主任医师 医科院肿瘤医院 胸外科212人已读
康晓征 副主任医师 医科院肿瘤医院 胸外科212人已读 - 学术前沿 晚期食管鳞癌免疫治疗“龙年新药”
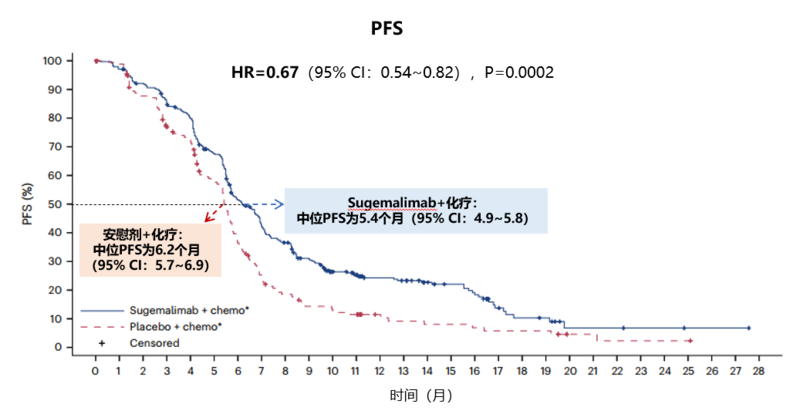
近年来,以免疫检查点抑制剂(PD-1/PD-L1抑制剂)为代表的免疫治疗为广大不可手术的晚期食管鳞癌患者开创了新希望。龙年将至,又一新药在晚期食管鳞癌中获得结果,提供了新选择。Sugemalimab(原名CS1001,中文通用名舒格利单抗)是一种全长、全人源免疫球蛋白G4(s228p)单克隆抗PD-L1抗体,已被中国国家药品监督管理局批准用于治疗III期和IV期非小细胞肺癌。相较于其它免疫检查点抑制剂,Sugemalimab的药效特点主要体现在其对Fcγ受体的结合能力上,使得Sugemalimab能够触发抗体依赖性细胞介导的吞噬作用(ADCP),即通过PD-L1+肿瘤细胞与巨噬细胞的交联促进肿瘤细胞的吞噬和清除。前期研究初步证实,Sugemalimab与5-氟尿嘧啶加顺铂联合使用在晚期食管鳞状细胞癌患者中显示出良好的客观缓解率和可管理的安全性。为明确Sugemalimab联合化疗作为晚期食管鳞状细胞癌患者的一线治疗的临床价值,我国学者开展了此项GEMSTONE-304研究。GEMSTONE-304是一项多中心、随机、双盲的3期临床研究(NCT04187352)。在2019年12月19日至2021年12月23日期间,在中国69个研究中心共计纳入了540名患有不可切除、局部晚期、复发或转移性食管鳞癌且未接受全身治疗的成年患者(18~75岁)。所有患者按2:1随机分组,接受Sugemalimab(n=358)或安慰剂(n=182)治疗,每3周一次,最多24个月;同时两组均接受化疗(顺铂+5-氟尿嘧啶),每3周一次,最多6个疗程。研究的两个主要终点分别是:(1)无进展生存期(PFS)和(2)总生存期(OS)。最终结果显示,安慰剂-化疗组和Sugemalimab+化疗组的中位PFS分别为5.4比6.2个月,Sugemalimab+化疗组的PFS期显著延长(P=0.0002)。安慰剂-化疗组和Sugemalimab+化疗组的中位OS分别为11.5比15.3个月,Sugemalimab+化疗组的OS期显著延长(P=0.0076)。在预先指定的亚组分析中,在大多数亚组中观察到与总体一致的OS改善。两组3级或以上治疗相关不良事件的发生率相当(51.3%比48.4%)。与安慰剂联合化疗相比,在不可切除、局部晚期、复发或转移性食管鳞癌患者中,Sugemalimab联合化疗(顺铂和5-氟尿嘧啶)显著延长患者PFS和OS,并且安全性可控。GEMSTONE-304研究结果可作为临床应用Sugemalimab联合化疗一线治疗晚期食管鳞癌的重要参考依据。参考文献:LiJ,ChenZ,BaiY,etal.First-linesugemalimabwithchemotherapyforadvancedesophagealsquamouscellcarcinoma:arandomizedphase3study.NatMed.PublishedonlineFebruary1,2024.doi:10.1038/s41591-024-02797-y
 康晓征 副主任医师 医科院肿瘤医院 胸外科37人已读
康晓征 副主任医师 医科院肿瘤医院 胸外科37人已读





